CAR-T:火箭已坠落,风筝还在飘
2016年12月4日,Kite Pharma宣布已经启动CAR-T疗法KTE-C19的BLA滚动申报,适应症为不适合自体干细胞移植的复发/难治性B细胞非霍奇金淋巴瘤。Kite希望在2017年第一季度完成BLA申请,并在当年上市。

Kite率先启动BLA申请
2016年12月4日,Kite Pharma宣布已经启动CAR-T疗法KTE-C19的BLA滚动申报,适应症为不适合自体干细胞移植的复发/难治性B细胞非霍奇金淋巴瘤。Kite希望在2017年第一季度完成BLA申请,并在当年上市。Kite同时宣布,KTE-C19有了正式名字:axicabtagene ciloleucel。如果一切顺利,Kite将完成超车,领先原来居先的Juno、诺华。
宾夕法尼亚大学、美国癌症研究院(NCI)、Fred Hutchinson癌症研究中心、纪念斯隆•凯特琳癌症中心、和西雅图儿童医院等是最早开展CAR-T细胞疗法的研究机构。2013年,Fred Hutchinson、纪念斯隆•凯特琳癌症中心和西雅图儿童医院的科学家联手成立了Juno。宾大则携手诺华开发CAR-T疗法。处在第一梯队的Kite原本则稍落后于Juno和诺华。三家企业的研发竞争可谓激烈。
Kite:副作用仍多,申报适应症有讲究
Kite的领先产品是KTE-C19,2016年9月26日,Kite Pharma公布KTE-C19的二期临床研究中期数据(ZUMA-1),疗效达到预期:弥漫性大B细胞淋巴瘤(DLBCL,51位患者)总体反应率ORR达到76%,完全缓解率CRR达到47%;转移滤泡性淋巴瘤(TFL,11名患者)总体反应率ORR达到91%,完全缓解率达到73%。Kite希望能在2017年上市该产品,尽管CMO仍保持谨慎态度,主要是KTE-C19仍存在一些严重的安全性问题:所有62名接受治疗的患者中,66%患者发生了较严重的(三级及以上)嗜中性粒细胞减少症,40%患者出现了较严重的贫血,29%患者出现粒细胞减少性发热,29%患者出现了血小板减少症,26%出现了脑病症状,还有2名患者思雨KTE-C19相关的副反应。此外,KTE-C19的疗效持续时间也是一个问题,3个月后总响应率和完全缓解率都出现明显下降,但是否如一期临床研究一样,3个月后的有效率不再发生明显变化,尚不得而知。
Kite此番BLA滚动申报(滚动申报是指临床研究尚未完成,基于已有数据申请上市,同时继续进行临床研究)颇为考究,选择的是无有效疗法的适应症。让人联想到2014年 Keytruda直接攻坚晚期黑色素瘤反超百时美施贵宝,手法使用的颇为老道。

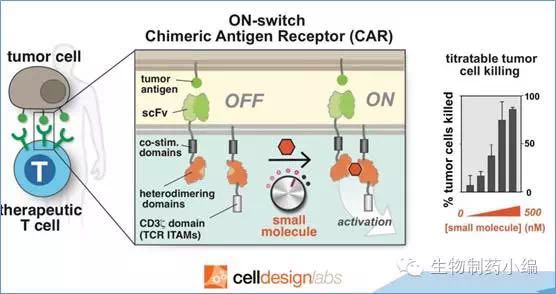
Kite与Cell Design Labs合作,引入小分子开关到新一代CAR-T疗法中。
诺华:稳扎稳打
2016年8月31日,诺华宣布解散细胞和与基因治疗部门,并入肿瘤研究部门。诺华宣诚CAR-T疗法的开发不收影响,但业界更倾向于相信诺华对CAR-T多少存在一些顾虑。
诺华的主打产品为CTL019,属于第二代CAR-T疗法,胞内信号区共刺激信号为CD-3zeta和CD137。最近的ASH会议上,诺华公布了临床2期ELIANA的数据,CTL019针对儿童和年轻人难治性/复发B-ALL的完全缓解率达到82%。副作用仍然严重,48%的患者出现了3(严重)到4(生命威胁)级的CRS,但没有出现治疗相关的死亡。15%的患者出现了3级神经毒性。
Juno:一波三折
宾夕法尼亚大学、美国癌症研究院(NCI)、Fred Hutchinson癌症研究中心、纪念斯隆•凯特琳癌症中心、和西雅图儿童医院等是最早开展CAR-T细胞疗法的研究机构。2013年,Fred Hutchinson、纪念斯隆•凯特琳癌症中心和西雅图儿童医院的科学家联手成立了Juno。宾大则携手诺华开发CAR-T疗法。
Juno在CAR-T细胞疗法领域与诺华、Kite处在第一梯队,并积极开展多项研发合作,保持技术领先及策略的灵活选择空间。Juno与纪念斯隆•凯瑟琳癌症研究中心(MSKCC,JACR015)、Fred Hutchison癌症研究中心(FHCRC,JACR014)、西雅图癌症研究所(SCRI,JACR017)积极开展合作,并在近两年先后收购了Stage Cell、AbVitro、Redox
Therapies三家生物科技公司,最近则与张峰创办的Editas签订合作协议,Juno一系列密集布局旨在加强CAR-T领域的布局。中国市场方面,Juno与药明康德成立合资公司,共同在中国推进其细胞疗法项目的开发。

2016年7月6日,JCAR015在针对成人复发或难治性B细胞急性淋巴细胞白血病的Ⅱ期临床试验中导致2例患者脑水肿死亡而被叫停,Juno在7月8日前递交修订材料,7月12日,FDA审核后排出JCAR015产品本身问题,许可JACR015继续临床试验。FDA快速反应的积极态度,将该事件的负面影响降到最低。11月23日,Juno再次宣布暂停JCAR015的临床研究,股价下滑逾30%。
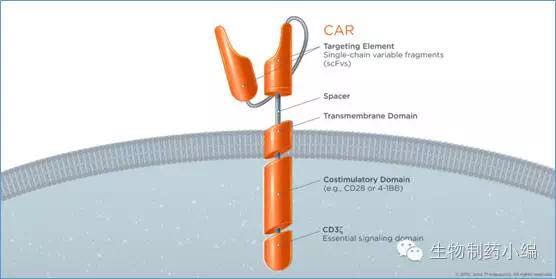
产品布局方面,第一梯队为靶向CD19的CAR-T疗法:JACR015、JACR017、JACR014。JACR015在纪念斯隆•凯特琳癌症研究中心开发,采用CD28作为共刺激因子,采用细胞为CD3+ PBMC,适应症为ALL、NHL;JACR017在西雅图癌症研究所开发,采用4-1BB作为共刺激因子,采用细胞为固定比例的CD8+ T细胞/CD4+ T细胞;适应症为儿科ALL、NHL;JACR014在Fred Hutchison癌症研究中心开发,采用细胞为固定比例的CD8+ T细胞/CD4+ T细胞。
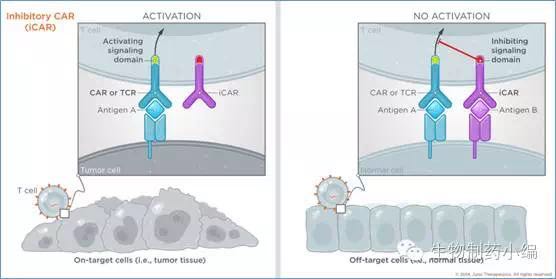
除此外,Juno积极开发升级版的CAR-T疗法:双特异性的CAR-T疗法。第二个特异性受体可以是激活型信号也可以是抑制性信号。以抑制性信号iCAR为例,设计为特异性识别健康组织中存在的靶标蛋白,如下图中的antigen B,癌症组织中,CAR识别antigen A杀伤癌细胞,正常组织中,antigen B结合iCAR,启动抑制信号,T细胞不会杀伤带有靶标antigen A的正常细胞。这样就提高了CAR-T疗法的特异性和安全性。
CD19之外,Juno也在积极开发其他靶点的CAR-T疗法,如CD22、WT1等靶点,以开发针对不同适应症的产品。
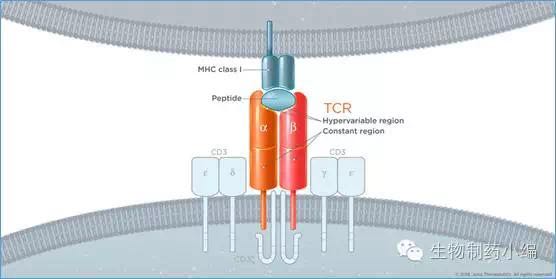
CAR-T疗法之外,Juno同时开发TCR-T疗法。
小编总结
CAR-T在B细胞淋巴瘤等适应症的颠覆性表现让资本趋之若鹜,然而Juno却两番折戟,促使大家更加冷静看待CAR-T,也给了Kite后来居上的机会。人体的免疫系统很神奇,却是一把双刃剑,必须谨慎对待副作用。CAR-T疗法公司纷纷布局新一代技术,给其安装分子开关,让疗效和副作用可控性更好。小编认为CAR-T技术本身前景看好,但工业界仍需要更多努力,在标准化上和成本控制室取得更大突破,才能真正提高药物可及性和市场接受度。
来源:生物制药小编
上一篇:黑磷纳米药物可多模式精准治疗癌症

